Kovalen 1Lihat jawabanIklanIklan claramatikaclaramatikaMata pelajaran KimiaKelas SMAKategori Ikatan KimiaKode kategori berdasarkan kurikulum KTSP 1074Kata kunci ikatan ion ikatan kovalenJawaban Perbedaan antara ikatan ion elektrovalen dengan ikatan kovalen antara lain Ikatan ion dapat terjadi karena perpindahan elektron dari. Senyawa di mana atom-atomnya berikatan secara kovalen Senyawa Kovalen Polar.

Ikatan Kovalen Non Polar Kovalen Polar Dan Kovalen Semi Polar Youtube
Berdasarkan kepolarannya senyawa kovalen terbagi menjadi senyawa kovalen polar dan senyawa kovalen non polar.

. Ikatan ion membentuk senyawa ion sedangkan ikata kovalen membentuk senyawa kovalen. Dapat terbentuk apabila unsur-unsur yang bereaksi mempunyai perbedaan daya tarik elektron yang cukup besar Perbedaan yang besar memungkinkan terjadi serah-terima. Senyawa kovalen koordinasi adalah ikatan kovalen di mana pasangan elektron yang dipakai bersama hanya disumbangkan oleh satu atom sedangkan atom yang satu lagi tidak menyumbangkan elektron.
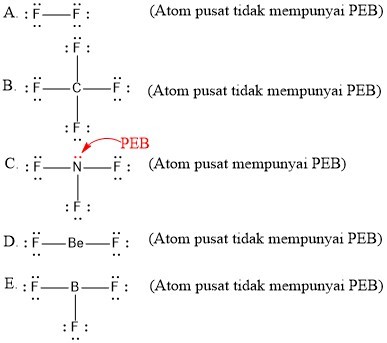
Dari gambar struktur lewis di atas maka senyawa yang berikatan kovalen polar adalah senyawa NH 3 HF dan H 2 O sedangkan senyawa yang berikatan kovalen nonpolar adalah CH 4. Senyawa kovalen berwujud lunak dan tidak mudah rapuh. Pada senyawa kovalen yang memiliki lebih dari dua unsur kepolarannya ditentukan oleh beberapa hal berikut ini.
Berikut ini ringkasan singkat perbedaan antara ikatan ion. Momen dipol akan timbul apabila senyawa kovalen tersebut tersusun dari dua atom dengan keelektronegatifan yang berbeda. Jumlah atom 2 harus berbeda.
Sebagai contoh atom-atom dalam air H2O disatukan oleh ikatan kovalen polar. Senyawa dapat berupa senyawa ionik dan senyawa kovalen tergantung pada jenis ikatan antara atom-atom penyusunnya. Ukuran Kuantitatif Titik Didih Senyawa Kovalen Senyawa polar titik didihnya lebih tinggi daripada senyawa non polar.
Perlu diingat baik-baik. Sebuah atom berfungsi sebagai pemberi pasangan. Ringkasan perbedaan Ikatan ion dan kovalen.
Kepolaran suatu senyawa dapat ditentukan dari perbedaan keelektronegatifan atom-atom yang membentuk suatu senyawa kovalen. Ikatan ini terjadi karena terjadinya penggunaan pasangan elektron yang digunakan secara bersamaan. Ikatan kovalen merupakan ikatan antar molekul non logam.
Senyawa ion dapat menghantarkan arus listrik dalam wujud lelehan dan larutan sedangkan senyawa kovalen polar hanya menghantarkan dalam bentuk larutan senyawa kovalen nonpolar tidak dapat menghantarkan sama sekali. Jelaskan perbedaan antara senyawa kovalen polar dengan kovalen nonpolar. Akan tetapi cara menggambarkan struktur lewis satu per satu terasa kurang efisien jika dalam soal terdapat lebih dari 5 jenis senyawa.
Dalam ikatan kovalen dikenal dengan adanya ikatan kovalen nonpolar dan polar. Pelarut 2020 Direktorat SMA Direktorat Jenderal PAUD DIKDAS dan DIKMEN 4 Modul Kimia Kelas X KD 38 PETA KONSEP. Jadi perbedaan sifat fisik senyawa ion kovalen dan logam adalah seperti uraian diatas.
Ikatan kovalen polar akan terjadi jika atom atom yang berikatan adalah heterointi. Ikatan kovalen koordinasi hanya dapat terjadi jika salah satu atom mempunyai pasangan elektron bebas PEB. Senyawa di mana atom-atomnya berikatan secara kovalen dan memiliki perbedaan keelektronegatifan Solute.
Zat terlarut Solvent. Jika momen dipol tidak sama dengan 0 senyawa kovalen tersebut merupakan senyawa kovalen polar. H2 N2 F2 2 Pasangan Elektron Bebas PEB Atom pusat memiliki pasangan elektron bebas PEB.
Perbedaan antara senyawa Polar dan Nonpolar sebagai berikut. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas.
Ikatan yang terjadi antara ion-ion logam dan non logam Ikatan terbentuk akibat gaya tarik listrik antara ion yang berbeda Ikatan ion juga dikenal sebagai ikatan elektrovalen. Ikatan kovalen koordinasi adalah ikatan yang terjadi jika pasangan elektron yang dipakai bersama hanya berasal dari satu atom saja sedangkan yang lain tidak menyumbangkan elektron. Ikatan antara unsur-unsur ini beragam bergantung pada jenis unsur.
Posted on 11 April 2022. Gula C6H12H6 Gas metana CH4 Diskusi. Atom N pada molekul amonia NH3 mempunyai.
Senyawa yang terbentuk akibat adanya suatu ikatan antar elektron pada unsur-unsur yang membentuknya. Senyawa kovalen memiliki titik didih dan titik leleh yang rendah. Senyawa kovalen bersifat polar apabila senyawa tersebut memiliki ciri-ciri sebagai berikut.
Senyawa kovalen memiliki ikatan kovalen. Dapat larut dalam air. Perbedaan antara Ikatan Kovalen Nonpolar dan Polar.
Tidak terdapat perbedaan keelektronegatifan. Jika jumlah momen dipol 0 senyawa kovalen tersebut merupakan senyawa kovalen nonpolar. Senyawa tersebut terbentuk karena unsur-unsur saling berikatan.
Juga senyawa kovalen dapat larut dalam air tetapi tidak berdisosiasi menjadi ion. Perbedaan Senyawa Polar dengan Non Polar. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik.
Anda dapat memprediksi ikatan kovalen akan terbentuk antara dua atom nonlogam. Secara garis besar ikatan antar unsur dibedakan menjadi dua jenis yaitu ikatan logam dan ikatan kovalen. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya.
Perbedaan Ikatan Kovalen Polar Ikatan Kovalen Nonpolar 1 Keelektronegatifan Terdapat perbedaan keelektronegatifan. Senyawa kovalen tidak memiliki bidang simetris seperti H 2 O dan NH 3. Senyawa polar adalah Senyawa yang terbentuk akibat adanya suatu ikatan antar elektron pada unsur-unsurnya.
HF asam florida. Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion-ionnya sehingga dapat menghantarkan arus listrik. Memiliki pasangan elektron bebas bentuk tdk simetris Berakhir ganjil kecuali BX3 dan PX5.
HF HCl dan HBr. Proses Mekanisme Terjadinya Kepolaran Senyawa Kovalen. Senyawa kovalen tidak dapat menghantarkan listrik.
Senyawa kovalen polar biasanya terjadi antara atom-atom unsur yang beda keelektronegatifannya besar mempunyai bentuk molekul asimetris dan mempunyai momen dipol tidak sama dengan nol 0. 3rb 50 1 rating AS. Jika dua atom nonlogam sejenis diatomik membentuk suatu senyawa kovalen misalkan H2 N2 Br2 dan I2 maka ikatan kovalen yang terbentuk memiliki keelektronegatifan yang sama atau tidak.
Jadi ikatan kovalen ini syaratnya ada molekul yang atom pusatnya mempunyai pasangan elektron bebas PEB. Senyawa Kovalen Polar dan Non-Polar Ikatan Kimia Bentuk Molekul dan Interaksi Antarmolekul. Senyawa kovalen mereka memiliki ikatan kovalen dalam strukturnya ikatan kovalen terbentuk ketika atom non-logam bersatu dan bersama-sama berbagi elektron.

Perhatikan Sifat Sifat Senyawa Berikut Yang T

Tabel Periodik Unsur Unsur Kimia Adolah Gambaran Unsur Unsur Kimia Dalam Bantuk Tabel Unsur Unsur Tasabu Periodic Table Chemistry Basics Life Hacks For School

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
10 Contoh Soal Dan Pembahasan Ikatan Kovalen Polar Dan Nonpolar Materi Kimia

Yang Termasuk Senyawa Non Polar Dari Senyawa Berikut Adalah

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya
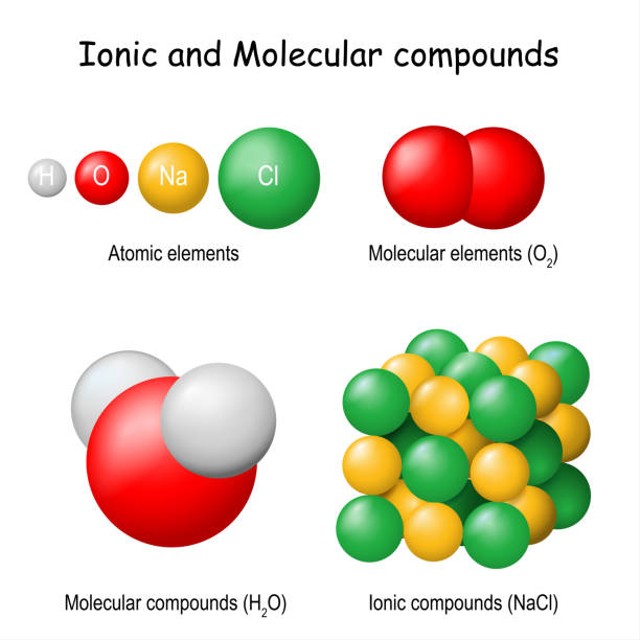
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com

1 Senyawa Kovalen Polar Dan Non Polar Ppt Download

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya

Trik Super Kilat Membedakan Senyawa Ion Dan Senyawa Kovalen Youtube

Senyawa Kovalen Polar Dan Non Polar Kimia Colearn

Sifat Senyawa Ion Kovalen Dan Polar Nonpolar Ikatan Kovalen Pdf
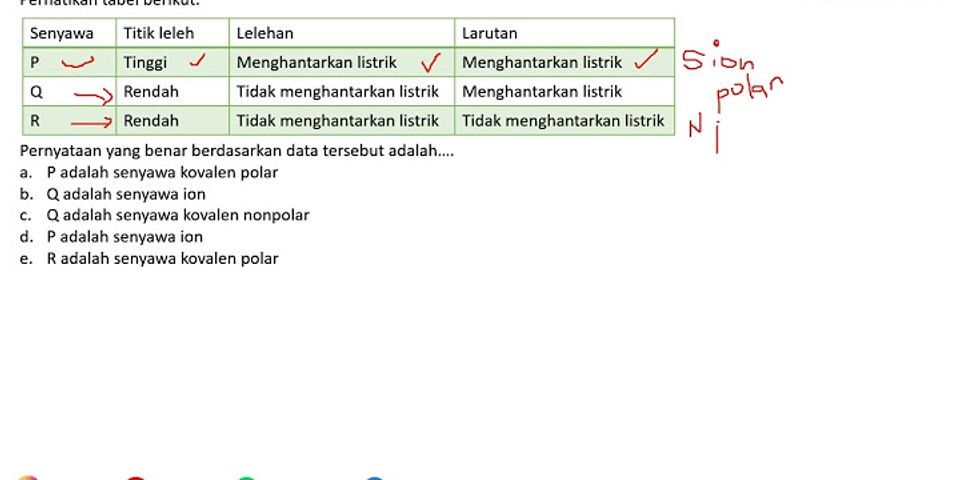
Mengapa Senyawa Ionik Dan Senyawa Kovalen Polar Dapat Menghantarkan Arus Listrik Jelaskan

Jelaskan Perbedaan Antara Senyawa Polar Dengan Nonpolar Dan Berikan Masing Masing Contohnya Brainly Co Id

Yang Termasuk Senyawa Non Polar Dari Senyawa Berikut Adalah

Perbedaan Polar Dan Nonpolar Apayangdimaksud Com

Kimia Kelas X Ikatan Kovalen Polar Non Polar Senyawa Kovalen Polar Dan Senyawa Kovalen Nonpolar Youtube


